Sour Gas Hydrate Formation Phase Behavior
A phase envelope with hydrate and water dew point curves is an excellent tool to find what phase water is in at operating conditions, during start-up, during shut-down and during upsets. In the November 2007 Tip of the Month (TOTM), we discussed the phase behavior of water-sour natural gas mixtures. In this tip, we will extend our study on the sour natural gas hydrate formation phase behavior. Specifically, we will study the impact of H2S and CO2 on the formation of hydrate in natural gas.
The hydrate formation temperature of a gas depends on the system pressure and composition. There are several methods of calculating the hydrate formation conditions of natural gases. At equilibrium, the chemical potential of water in the hydrate phase is equal to that in each of the other coexisting phases. Parrish and Prausnitz [1] developed a thermodynamic model to describe this phenomenon, and later, the model was improved by Holder et al. [2]. These methods are suitable for calculations using a computer with equations of state. The details of hand calculation methods can be found in Chapter 6 of Volume 1 [3] of “Gas Conditioning and Processing” and Chapter 20 of GPSA DATA BOOK [4]. In this work we will use the Soave-Redlich-Kwong (SRK EoS) [5] in ProMax [6] software.
Equilibrio de Fases Formación de Hidratos en Gases Agrios
Una envolvente con curvas de punto de rocío de agua e hidratos es una excelente herramienta para verificar la fase de agua en condiciones operativas, de arranque, cierre, y durante los inconvenientes. En el Previo del Mes (PDM) de Noviembre 2007, hemos discutido el comportamiento de fases de las mezclas de agua más gas agrio. En este previo, extenderemos nuestra investigación hacia el comportamiento de fases de los gases agrios con formación hidratos. Específicamente estudiaremos el impacto del H2S y CO2 sobre la formación de hidratos en un gas natural.
La formación de hidratos de un gas natural depende de la presión y composición del sistema. Existen varios métodos para el cómputo de estas condiciones de formación en l gas natural. En condiciones de equilibrio, el potencial químico del agua en la fase hidratada es igual al mismo en cada una de las fases coexistentes. Parrish, y Prausnitz [1] desarrollaron un modelo termodinámico para describir este fenómeno, y mas luego, el modelo fue actualizado por Holder, et. al. [2]. Estos métodos son aplicables para los cómputos aplicando las ecuaciones estado. Los detalles de los cálculos efectuados a mano se pueden encontrar en el Capítulo 6 del Volumen I [3] del “Gas Conditioning and Processing”, y el Capítulo 20 del Volumen de Datos GPSA [4]. En este trabajo aplicaremos la EDE Soave-Redlich-Kwong (SRK EoS –EDE) [5] en la herramientas de computo (software) ProMax [6].
The compositions of the gas mixture studied in this study are shown in Table 1.
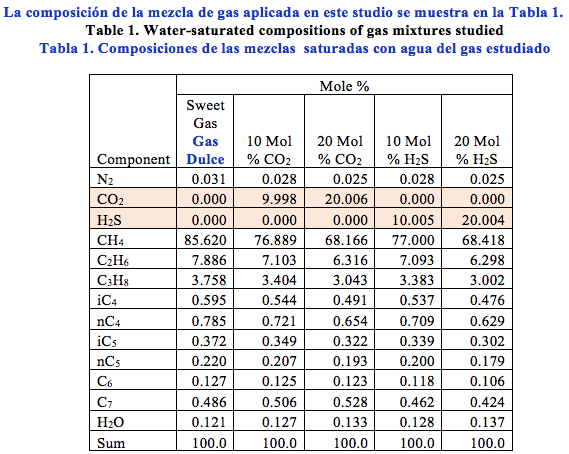
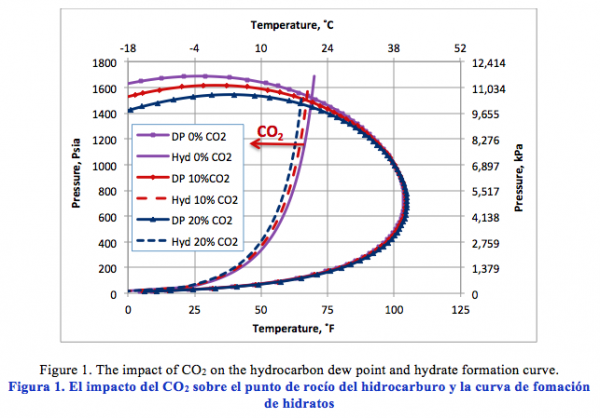
Figure 1 presents the calculated hydrate formation curve (solid curve) and the dew point portion of the phase envelope of a sweet natural gas (solid curve with the square). Figure 1 also presents the dew point and hydrate formation curves for the same gas mixture containing 10 and 20 mole % CO2. Figure 1 indicates that as the CO2 mole % increases from 0 to 20 mole %, the hydrate formation curves shift slightly to the left, depressing the hydrate formation temperature. Note that the points to the left and above the hydrate curves represent the hydrate formation region. From an operational point of view, this region should be avoided/prevented. This figure also indicates, as CO2 mole % increases, the cricondenbar decreases and the phase envelope shrinks.
La Figura 1 presenta la curva calculada para la formación de hidratos (curva sólida) más la porción de la curva del punto de rocío de la envolvente de un gas natural dulce (curva sólida con los cuadros). La figura 1 igual presenta el punto de rocío más la curva de formación de hidratos para le mismo gas conteniendo 10 y 20 % de CO2. La Figura 1 indica que mientras el porcentaje molar del CO2 aumenta de 0 a 20 %, la curva de formación de hidratos se desplaza ligeramente hacia la izquierda, deprimiendo la temperatura de formación de los hidratos. Nótese que los puntos a la izquierda y por encima de ésta curva representa la región de formación de hidratos. Desde un punto de vista operacional, ésta región debe evitarse/prevenirse. Esta figura igual indica que, mientras el % molar del CO2 aumenta, la cricondenbara disminuye, y se achica el diagrama de fases.
Similarly, Figure 2 presents the calculated hydrate formation curve (solid curve) and the dew point portion of phase envelope for the same sweet natural gas (solid curve with the square). Figure 2 also presents the dew point and hydrate formation curves for the same gas mixture containing 10 and 20 mole % H2S. Figure 2 indicates that as the H2S mole % increases from 0 to 20 mole %, the hydrate formation curves shift considerably to the right, promoting the hydrate formation temperature. This is opposite to the effect of CO2 and it is more pronounced. From an operational point of view, this is undesirable because H2S expands the hydrate formation region to the right. Note that the points to the right and below of the hydrate curve represent the hydrate-free region. Figure 2 also indicates, as H2S mole % increases, the cricondenbar decreases and the phase envelope shrinks. The shrinkage of the phase envelope is less than that of CO2.
De manera similar, la Figura 2 presenta la curva calculada para la formación de hidratos (curva sólida con los cuadros). Ésta también presenta el punto de rocío y la curva de formación de hidratos para la mezcla conteniendo 10 y 20 % molar del H2S. La Figura 2 indica que mientras el % molar del H2S aumenta de 0 a 20 %, la curva de formación de hidratos de desplaza hacia la derecha, favoreciendo la temperatura de formación de los hidratos. Esto es lo opuesto del CO2 y se observa más pronunciado. Desde le punto de vista operacional, esto es indeseable por cuanto el H2S amplia la región de formación de los hidratos hacia la derecha. Nótese que los puntos de la derecha y por debajo de la línea de los hidratos representa la región libre de los mismos. La Figura 2 también indica que, mientras el % molar del H2S incrementa, la cricondenbara disminuye y se achica la región del diagrama de fases. Ésta reducción se observa menor que la relacionada con el CO2.
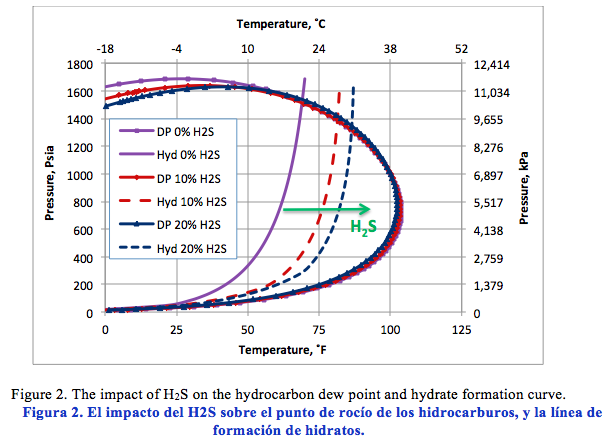
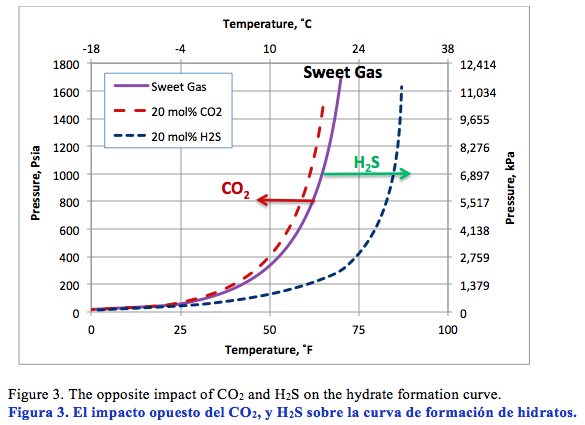
Figure 3 presents the calculated hydrate formation curves for a sweet gas, a sour gas with 20 mole % CO2 and a sour gas with 20 mole % H2S. This figure clearly indicates that the impact of H2S is much bigger than the CO2 impact; CO2 depresses (shifts to the left) the hydrate formation condition slightly but H2S promotes hydrate formation considerably. As an example, at 1000 psia (6900 kPa), CO2 reduces hydrate formation temperature for this gas by about 5.5˚F (3˚C) while, H2S increase hydrate formation temperature by about 20˚F (11.1˚C).
La Figura 3 presenta las curvas calculadas para la formación de hidratos relacionadas con un gas natural dulce, un gas agrio con 20 % molar del CO2, y un gas agrio con 20 % molar del H2S. Esta figura indica claramente que le impacto del H2S es mucho mayor que el impacto del CO2; éste deprime (desplaza a la izquierda) ligeramente la condición de formación de hidratos, pero el H2S promueve esta condición considerablemente. Como ejemplo, a 1000 lpca (6900 kPa), el CO2 reduce la temperatura de hidratación de este gas por unos 5.5 ᴼF (3ᴼC), mientras que el H2S aumenta la misma por unos 20 ᴼF (11.1ᴼC).
Conclusions:
The presence of CO2 and H2S in natural gas has an opposite impact on the hydrate formation condition. While the impact of CO2 is small, H2S has considerable impact on the hydrate formation condition. CO2 depresses hydrate formation (acts as hydrate inhibitor and shifts the hydrate curve to the left) while H2S shifts the hydrate curve to the right, promotes hydrate formation conditions, and may cause severe operational problems.
Conclusiones:
La presencia del CO2, y el H2S en un gas natural promueven un impacto opuesto sobre las condiciones de formación de hidratos. Mientras que éste es ligero para el CO2, el H2S impacta considerablemente las condiciones de formación de los hidratos. El CO2 deprime la formación de hidratos (actúa como inhibidos, y desplaza la curva de hidratación hacia la izquierda), mientras que el H2S desplaza la curva de hidratación hacia la derecha, promoviendo la condiciones de formación, y puede ser el causante de severo problemas operacionales.
To learn more about similar cases and how to minimize operational problems, we suggest attending our G40 (Process/Facility Fundamentals), G4 (Gas Conditioning and Processing), P81 (CO2 Surface Facilities), and PF4 (Oil Production and Processing Facilities) courses.
Para informarse adicionalmente sobre casos similares y como minimzar los problemas operacionales, sugermios su asistenca a nuestras sesiones G40 (Process/Facility Fundamentals), G4 (Gas Conditioning and Processing), P81 (CO2 Surface Facilities), and PF4 (Oil Production and Processing Facilities).
John M. Campbell Consulting (JMCC) offers consulting expertise on this subject and many others. For more information about the services JMCC provides, visit our website at www.jmcampbellconsulting.com, or email us at consulting@jmcampbell.com.
La Consultoría John M. Campbell (JMCC) ofrece experiencia de consultoría en este tema y muchos adicionales. Para mayor información sobre éstos servicios ofrecidos, visite nuestra dirección en la red al www.jmcampbellconsulting.com, o envíenos su correo a consulting@jmcampbell.com.
By: Dr. Mahmood Moshfeghian
Traducido al Español por: Dr. Frank E. Ashford
Reference:
- Campbell, J.M., “Gas conditioning and Processing, Vol 1: The Basic Principles”, 8th Edition, Edited by R.A. Hubbard, John M. Campbell & Company, Norman, USA, 2001.
- Parrish, W.R., and J.M. Prausnitz, “Dissociation pressures of gas hydrates formed by gas mixtures,” Ind. Eng. Chem. Proc. Dev. 11: 26, 1972.
- Holder, G. D., Gorbin, G. and Papadopoulo, K.D, “Thermodynamic and molecular properties of gas hydrates from mixtures containing methane. argon, and krypton,” Ind. Eng. Chem. Fund. 19(3): 282, 1980.
- Gas Processors Suppliers Association; “ENGINEERING DATA BOOK” 13th Edition – FPS; Tulsa, Oklahoma, USA, 2012.
- G. Soave, Chem. Eng. Sci. 27, 1197-1203, 1972.
- ProMax 3.2, Bryan Research and Engineering, Inc, Bryan, Texas, 2012.

No comments yet. You should be kind and add one!
By submitting a comment you grant Campbell Tip of the Month – Spanish a perpetual license to reproduce your words and name/web site in attribution. Inappropriate and irrelevant comments will be removed at an admin’s discretion. Your email is used for verification purposes only, it will never be shared.