La mejor manera de prevenir la formación (y corrosión) debido a la formación de los hidratos es la mantener el caño, la tubería, y los equipos libres de agua líquida. Existen ocasiones, correctas o incorrectas, cuando se toma la decisión de operar una línea o proceso que contiene agua líquida. Si es esta la decisión, y la temperatura del proceso es menor que la de hidratación, es precisa la inhibición de esta agua.
Se pueden agregar muchas sustancias al agua para deprimir tanto la temperature de hidratación así como la de congelamiento. A causa de muchas razones prácticas un inhibidor termodinámico (THI – ITH) tal como el alcohol o uno de los glicoles es inyectado, usualmente el metanol, dietilén glicol (DEG), o monoetilén glicol (MEA). Todos pueden ser recuperados y recirculados, pero el ambiente económico para la recuperación del metanol puede que no sea favorable en todas aplicaciones. La inhibición con metanol y o los glicoles puede incurrir gastos apreciables debido a la alta dosificación requerida (10 % a 60% de la fase acuosa). Altas concentraciones de solventes el incrementan el potencial de escamas por cuanto se reduce la solubilidad de las sales de formación de escamas, y precipitan la mayoría casi todos los inhibidores conocidos. La tasa total del inhibidor requerido es la cantidad/concentración deseada para lograr la supresión de los hidratos, así como la cantidad del inhibidor que se concentrarán en las fases de vapor y líquida del hidrocarburo.
El inhibidor presente en la fase gaseosa o la líquida proporciona poco impacto sobre las condiciones de formación de hidratos. Debido a las limitaciones en la certeza de los cómputos de depresión en la temperatura de hidratación, y distribución de flujo en el proceso, se recomienda que la temperatura de formación de hidratos con inhibición se logre con un factor de diseño por debajo de la mínima temperatura de operación, para asegurar caudales adecuados del inhibidor.
Es muy importante la determinación la cantidad y concentración de los inhibidores en las distintas fases por razones prácticas más las aplicaciones industriales. De manera que, para determinar la cantidad y concentración requerida de estos inhibidores, se han desarrollado varios modelos aplicables para los cómputos manuales, así como aquellos destinados para su incorporación dentro del ambiente de modelaje computacional.
Inhibidores de baja dosificación son relativamente nuevos solo habiendo logrado recientemente la etapa de “tecnología comprobada” en el procesamiento del petróleo y gas. Mientras que estos sistemas desplazan la línea de formación de hidratos hacia la izquierda, esto solo es temporal. En sistemas típicos éstos “retardarán” la formación de hidratos por unas 12 horas. Inhibidores de baja dosificación (LDHIs) son dos clases de químicos: Inhibidores Cinéticos (KHI’s), y Anti-Aglomerantes (AA’s). Un KHI pude prevenir la formación del hidrato pero no puede disolver uno ya establecido. Lo KHIs disponibles presentan ciertas dificultades controlando una temperatura umbral subenfriada (ΔT) de 15 °C (27 °F). Los AA’s permiten la formación de los hidratos con una dispersión estable de los cristales en el hidrocarburo líquido.
Los AA’s generan agua estable dentro de una micro-emulsión de petróleo. Los AA’s son absorbidos en los látices cristalinos del hidrato e impiden el crecimiento adicional del cristal, pero éstos deben contar con una fase líquida del hidrocarburo que refleje una relación agua crudo de 40 – 50%.
Los estudios de laboratorio y experiencia en el campo indican que la sinergia hidrato – inhibición se adquiere a través de la combinación de dos o más de los THI’s [1], o un THI mas LDHI [2]. Esto se determina como la inhibición híbrida de hidratos (HHI).
En este PDM demostraremos el efecto sinergético de los THI’s como la solución del NaCl, y MEG. En el próximo PDM, trataremos los resultados de una aplicación exitosa del metanol y una solución de KHI para un pozo produciendo gas natural, condensado, y agua en el Golfo de México, (GOM).
THI’s combinados (MEG+NaCl, o MEG + KCl)
El agua de producción de los yacimientos de gas contiene una solución electrolítica tal como el NaCl, KCl, y CaCl2. Para poder estimar la temperatura de formación de los hidratos en la presencia de los inhibidores mixtos termodinámicos, proponemos sumar las temperaturas de depresión asociadas con cada inhibidor individual. Los pasos se resumen abajo:
- Usando el método descrito en la referencia [3], se estima la temperatura de formación de hidratos en presencia del agua pura, To.
- Aplicando un método similar la de Javanmardi , et al [1], se estima la temperatura de depresión de hidratos debido a la presencia de la solución salina, sal ΔT.
- Usando un método similar al de Hammerschmidt [4], ese estima la depresión de la temperatura de hidratación debido a la presencia de una solución del MEG, MEG ΔT.
- Se suma el ΔT de la sal y el MEG ΔT, ΔT Total.
- La temperatura de formación de hidratos se calcula restando el ΔT total del To.
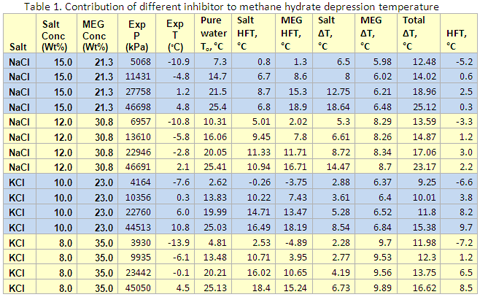
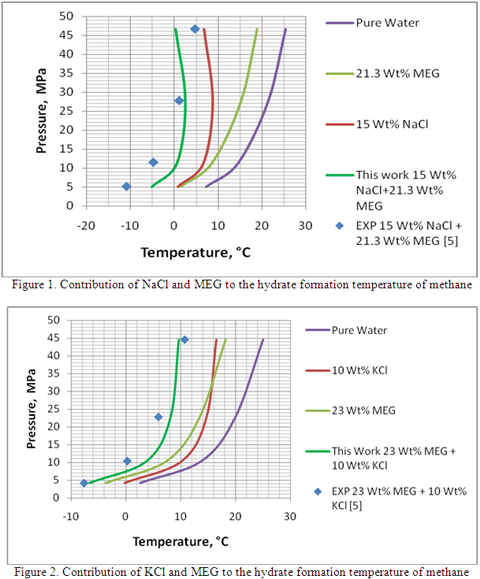
Como ejemplo., la Tabla 1 presenta el detalle de cómputo y la contribución de cada inhibidor a la temperatura de formación de hidratos para el gas metano a distintas presiones y concentraciones de inhibidor mezclado. Una comparación con la temperatura de formación de hidratos (última columna de la Tabla 1) con data experimental (la quinta columna) medida por Masoudi et. al. [5] indica una correspondencia relativamente buena. Las Figuras 1, y 2 también presentan al contribución de cada inhibidor a la temperatura de formación de los hidratos como descrita arriba para una solución de NaCl + MEG , y KCl + MEG, respectivamente.
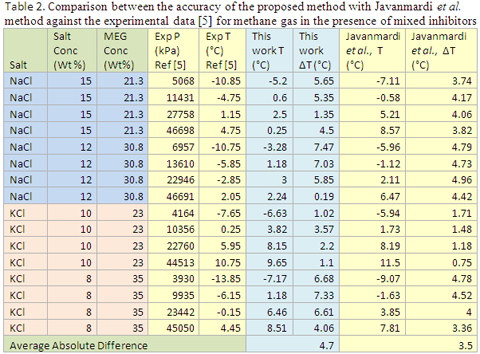
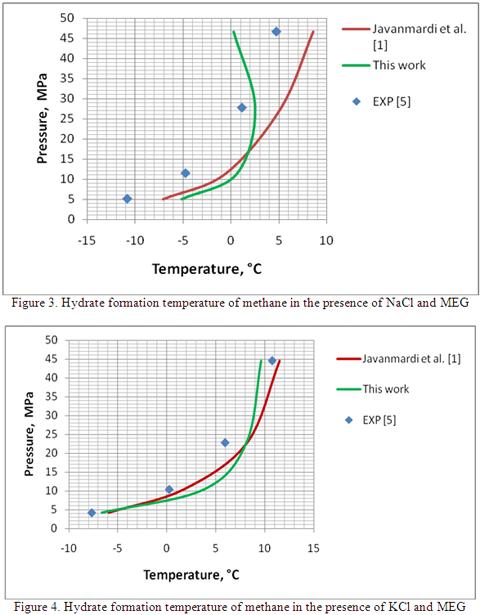
La Table 2 presenta una comparación entre la certeza del método propuesto con el de Javanmardi et. al. Aplicando la data experimental del gas metano en la presencia de inhibidores mezclados. La Tabla 2 también indica una diferencia en la temperatura ponderada absoluta de 4.7 y 3.5 °C para el método propuesto y el de Javanmardi, et. al. respectivamtne.
En resumen, se propone un procedimiento sencillo para la estimación de la temperatura de formación de hidratos en la presencia de los THI’s tales como MEG, y una solución de sal. Este procedimiento se puede usar para una mezcla de glicol, y solucione electrolíticas. El mismo es relativamente sencillo y su certeza es suficientemente razonable para los cómputos de facilidades. Para predicciones de mayor certeza para la temperatura de formación de hidratos en la presencia de electrolitos, los lectores deben referirse a los trabajos presentados por Javanmardi, et. al. [1] , y Masoudi, et. Al. [5].
Para informarse adicionalmente sobre casos similares y como minimizar problemas operacionales sugerimos su asistencia a los cursos; G4 (Gas Conditioning and Processing) and G5 (Gas Conditioning and Processing – Special).
La Consultoría JMC está en capacidad para ofrecerl pericias termodinámicas en los proyectos de procesamiento del gas para asegurar que el modelo de procesos desarrollado sea el de mayor precisión posible. Con los Consultores mas solicitados en la Industria del Petróleo y Gas, la Consultoría John M. Campbell proporciona la primera selección en los servicios de consultoría para clientes selectos. Para mayor información sobre los servicios ofrecidos por Campbell, visite nuestra dirección de red a Campbell Consulting.
By: Dr. Mahmood Moshfeghian
Traducido al Español Por: Dr. Frank E. Ashford
Reference:
- Javanmardi, J., Moshfeghian, M. and R. N. Maddox, “An Accurate Model for Prediction of Gas Hydrate Formation Conditions in Mixture of Aqueous Electrolyte Solutions and Alcohol,”Canadian J. of Chemical Engineering, 79, 367-373, (2001).
- Szymczak, S., Sanders, K., Pakulski, M., Higgins, T.; “Chemical Compromise: A Thermodynamic and Low-Dose Hydrate-Inhibitor Solution for Hydrate Control in the Gulf of Mexico,” SPE Projects, Facilities & Construction, (Dec 2006).
- Campbell, J. M., “Gas Conditioning and Processing”, Vol. 1, The Basic Principles, 8th Ed., Second Printing, J. M. Campbell and Company, Norman, Oklahoma, (2002).
- Hammerschmidt, E. G. “Formation of Gas Hydrate in Natural Gas Transmission Lines”, Ind. Eng. Chem., 26, 851-855, (1934).
- Masoudi, R., Tohidi, B., Anderson, R., Burgass, R., and Yang, J. “Experimental Measurement and Thermodynamic Modelling of Clathrate Hydrate Equilibria and Salt Solubility in Aqueous Ethylene Glycol and Electrolyte Solutions,” Fluid Phase Equilibria, 219, 157-163 (2004).

No comments
Trackbacks
By submitting a comment you grant Campbell Tip of the Month – Spanish a perpetual license to reproduce your words and name/web site in attribution. Inappropriate and irrelevant comments will be removed at an admin’s discretion. Your email is used for verification purposes only, it will never be shared.